葡萄糖(GO)检测试剂盒产品中文说明书
2020.03.02 点击4698次
(本中文说明书为翻译稿,仅供参考,应以英文版为准) 货号:3091314 (Sigma-Aldrich : GAGO20) 储存温度:2-8℃ 产品描述: 酶作为一种分析工具,在食品、生化和制药工业中得到了广泛的应用。酶的方法是特异性的,可重复的,灵敏的,快速的,因此,是分析目的的理想方法。由于酶的高特异性和敏感性,定量分析可以在很少或没有样品准备的情况下进行1-5。 本试剂盒用于食品和其它材料中葡萄糖的定量、酶法测定。各种出版物已经报道了在不同的系统和样本上使用该试剂盒,包括果蝇6-8、牛粪9、培养的小鼠肌肉细胞10、HEPG2细胞11和水生生物12。 原理:
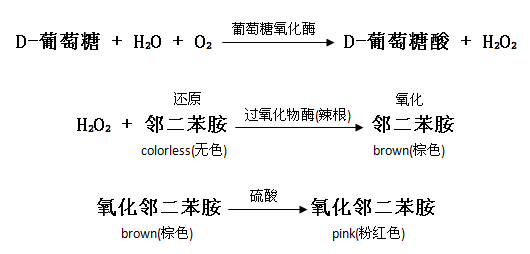
• 葡萄糖氧化酶将葡萄糖氧化成葡萄糖酸和过氧化氢。 • 过氧化氢在过氧化物酶的存在下与邻二苯胺反应生成有色产物。 • 氧化的邻二苯胺与硫酸反应生成更稳定的有色产品。 • 在540 nm处测得的粉红色的强度与原始葡萄糖浓度成正比。 试剂盒组成: 1、葡萄糖氧化酶/过氧化物酶试剂 • 将未打开的试剂盒试剂保存在2-8℃。每个胶囊包含500单位的葡萄糖氧化酶(黑曲霉),100单位(purpurogallin units)的过氧化物酶(辣根)和缓冲盐。 • 将胶囊内容物倒入琥珀色的瓶子中。 • 将这些物质溶解在39.2 mL去离子水中。 • 该溶液在2-8℃最多稳定一个月,在-20℃冷冻至少六个月。 • 如果出现浑浊,请丢弃。 2、邻二苯胺试剂 • 将未打开的试剂盒试剂保存在2-8℃。尽量减少曝光。预先称量的小瓶中含有5毫克的邻二苯胺盐酸盐。 • 用1.0 mL的去离子水重新配制邻二苯胺小瓶的内容物。 • 翻转样品瓶几次以溶解。 • 避免将试剂暴露在光线下。 • 溶液在2-8℃下稳定3个月。 3、分析试剂 • 向装有39.2 mL葡萄糖氧化酶/过氧化物酶试剂的琥珀瓶中加入0.8 mL邻二苯胺试剂。 • 将瓶子倒过来几次混合。 • 尽量减少暴露在光线下。 • 溶液在2-8℃下稳定1个月。 • 如果出现浑浊或其他颜色,请丢弃。 4、葡萄糖标准溶液 • D-葡萄糖,在0.1%的苯甲酸中为1.0 mg/mL。 • 该标准可追溯到NIST标准,并提供即用型。 • 在2-8℃稳定至少六个月。 • 如果出现混浊,请丢弃。 必需但未提供试剂: 硫酸,ACS试剂,为18M硫酸试剂。在去离子水中准备6M溶液。 仪器: 1、分光光度计或比色计:可在540nm下测定吸光度。 2、比色皿。 3、试管,18 mm×150 mm 4、移液器:能够准确分配20 μL至2.0 mL的体积。 5、能保持温度在37℃的水浴锅 注意事项和免责声明: 本试剂仅供科研使用,不能用于药品、家庭以及其他用途。有关危险和安全操作规程的信息,请参阅安全数据表。 操作步骤: 样品制备: 液体: • 用去离子水将样品稀释至葡萄糖浓度为20-80μg/mL。 • 如有必要,对溶液进行过滤或去蛋白处理以使其澄清。 • 样品葡萄糖含量较低且颜色较深时,应予以脱色处理。 • 含碳酸或发酵样品,须脱气处理。 固体: • 称量0.1mg样品。 • 用去离子水提取样品。可以将溶液加热(<75℃)以帮助萃取。 • 用去离子水稀释提取液品至葡萄糖浓度为20-80μg/mL。 • 如有必要,对溶液进行过滤或去蛋白处理以使其澄清。 测定: 方法1:标准曲线中的葡萄糖浓度 1、吸取以下溶液到相应的试管中:
2、计时起点,通过向第一个试管中加入2.0 mL的测定试剂开始反应并混合。在向每个后续试管中添加测定试剂之间,要间隔30至60秒。 3、让每个试管在37℃下反应30分钟。通过在每个试管中加入2.0 mL的6M硫酸溶液,以30-60秒的间隔停止反应。小心地将各管彻底混合。 4、在540 nm处测量每个试管对空白试剂的吸光度。 方法2:单一标准品中的葡萄糖浓度 1、吸取以下溶液到相应的试管中:
2、计时起点,通过向第一个试管中加入2.0 mL的测定试剂开始反应并混合。在向每个后续试管中添加测定试剂之间,要间隔30至60秒。 3、让每个试管在37℃下反应30分钟。通过在每个试管中加入2.0 mL的6M硫酸溶液,以30-60秒的间隔停止反应。小心地将各管彻底混合。 4、在540 nm处测量每个试管对空白试剂的吸光度。 结果: 计算方法1: 对于标准品,绘制540 nm处的吸光度(y轴)与葡萄糖的毫克含量(x轴)标准曲线。如果标准曲线不是线性的,则结果将不准确。重复测定。 对于测试,从标准曲线确定葡萄糖毫克数。 将上面确定的毫克葡萄糖乘以样品制备中的稀释倍数。 计算方法2:
将上面确定的毫克葡萄糖乘以样品制备中制备的稀释倍数。 参考文献: 1、Bergmeyer, H.U. and Bernt , E., Methods of Enzymatic Analysis (H.U. Bergmeyer, ed.). Academic Press (New York, NY), 2nd ed., pp. 1205-1212 (1974). 2、Official Methods of Analysis, 16th Edition. AOAC International, Sections 32.2.05 and 44.7.12 (1995). 3、Raabo, E. and Terkildsen, T.C., Scand. J. Clin. and Lab. Invest., 12(4), 402-407 (1960). 4、Southgate, D.A.T., Determination of Food Carbohydrates. Applied Science Publishers, Ltd. (London, 1976). 5、Washko, M.E. and Rice, E.W., Clin. Chem., 7(5), 542-545 (1961). 6、Wen, Z. et al., Appl. Biochem., Biotechnol., Spring; 121-124, 93-104 (2005). 7、Huang, J.-H. and Douglas, A.E., Biol. Lett., 11(9), 20150469 (2015). 8、Unckless, R.L. et al., G3 (Bethesda), 5(3), 417-425 (2015). 9、Tennessen, J.M. et al., Methods, 68(1), 105-115 (2014). 10、Hien, T.T. et al., J. Biol. Chem., 291(7), 3552-3568 (2016). 11、Whitehead, T.D. et al., J. Nucl. Med., 54(10), 1812-1819 (2013). 12、Hsiao, C.J. et al., Dis. Aquat. Organ., 119(3), 199-206 (2016). | 产品分类
最新文章
最新产品
友情链接
|
 |